Introduction
Thrombose veineuse superficielle et thromboembolie veineuse: une grande étude épidémiologique prospective.
Évaluer la prévalence de la thromboembolie veineuse chez les patients atteints de SVT et déterminer l’incidence à trois mois de complications thromboemboliques
Parmi les 844 patients atteints de SVT à l’inclusion (âge médian, 65 ans, 547 femmes), 210 (24,9%) ont également eu une thrombose veineuse profonde (TVP) ou une embolie pulmonaire symptomatique. Parmi les 600 patients sans TVP ou l’embolie pulmonaire à l’inclusion qui étaient admissibles à un suivi de 3 mois, 58 (10,2%) ont développé des complications thromboemboliques à 3 mois (embolie pulmonaire, 3 [0,5%], TVP, 15 [2,8%]; Extension de SVT, 18 [3,3%] et récurrence de SVT, 10 [1,9%]), malgré 540 patients (90,5%) ayant reçu des anticoagulants. Les facteurs de risque de complications à 3 mois étaient le sexe masculin, l’histoire de la TVP ou l’embolie pulmonaire, le cancer antérieur et l’absence de varices.
Les thromboses veineuses superficielles (TVS) des membres inférieurs ont longtemps été considérées comme une pathologie bénigne voire une simple complication de la maladie variqueuse. il existe 20 % d’extension du thrombus vers le réseaux profond, avec embolie pulmonaire, les causes sont identique à une thrombose veineuse superficielle ,elle sont bénigne s’il n’ya pas d’extension,avec une guerison totale
Des travaux récents permettent de mieux appréhender leur histoire naturelle et leur gravité potentielle, et de mieux définir leur place au sein de la maladie thromboembolique veineuse (TEV), à côté des thromboses veineuses profondes (TVP) et des embolies pulmonaires (EP).
Les TVS sont considérées comme étant une pathologie fréquente, mais leur incidence exacte demeure mal connue dans la population adulte. Une étude française récente [1] a montré une incidence annuelle plus faible que celle attendue : 0,6 %, soit environ la moitié de l’incidence annuelle des TVP (1,2 %) et du même ordre de grandeur que l’incidence annuelle des EP (0,6 %).
Leur approche thérapeutique a été profondément modifiée ces dernières années. Les anti-inflammatoires, autrefois largement prescrits, ont laissé la place aux anticoagulants. La compression élastique demeure un élément important du traitement.
Étiopathogénie des thromboses veineuses
Il est habituel de distinguer les TVS survenant sur veines variqueuses et les TVS survenant sur des veines non variqueuses. Cette dernière situation est souvent secondaire à un état inflammatoire, une maladie générale ou à l’existence d’une thrombophilie.
Épidémiologie des TVS
Deux grandes études épidémiologiques récentes [2,3], ont montré qu’au moment du diagnostic, une TVP était associée à une TVS dans 25 % des cas environ et une EP dans 4 à 5 % des cas.
Par ailleurs, des récidives TEV après TVS surviennent dans 3 à 20 % des patients, en fonction de la durée du suivi. Elles peuvent prendre la forme d’une nouvelle TVS, mais également d’une TVP ou d’une EP. Ces données épidémiologiques montrent la place des TVS au sein de la maladie TEV et leur gravité potentielle.
Devant une suspicion clinique de TVS, la réalisation d’un examen écho-doppler en urgence est indispensable afin :
- D’affirmer le diagnostic de TVS (figure 1). Si le diagnostic clinique est souvent évocateur en présence d’un cordon induré et inflammatoire, des diagnostics différentiels sont possibles.
- Définir la localisation précise et l’extension de la TVS, extension souvent sous-estimée à l’examen clinique notamment au 1/3 supérieur de la cuisse et à la fosse poplitée, alors qu’une extension à la jonction saphéno-fémorale ou saphéno-poplitée est un critère de gravité comportant un risque d’EP.
- De rechercher une éventuelle TVP associée (qui peut être à distance de la TVS y compris sur le membre inférieur controlatéral).
Traitement des thromboses veineuses superficielles
Historiquement, les AINS étaient largement utilisés, per os et/ou en applications locales.
A partir de la prise de conscience que les TVS faisaient intégralement partie de la maladie TEV et étaient un facteur de risque de TVP, les AINS ont laissé la place aux anticoagulants. Cependant jusqu’à très récemment, plusieurs études contrôlées randomisées avaient échoué à clairement démontrer l’efficacité d’un protocole thérapeutique basé sur les anticoagulants. Ceux-ci étaient alors utilisés de façon très variable par les praticiens en fonction de leur « feeling » : HBPM à doses préventives de durées variables, à doses curatives, avec un relais par les AVK, etc… [2]
Si les premières études contrôlées et randomisées n’ont pas permis de définir un protocole thérapeutique précis, elles ont fourni des informations importantes, à savoir :
- Les traitements anticoagulants utilisés sur une courte durée (10 jours) ou moyenne (30 j), à doses préventives comme curatives, semblaient insuffisants, car un phénomène de rebond, caractérisé par la survenue d’évènements TEV, était observé durant la période de suivi.
- L’absence de bénéfice d’un traitement à doses curatives versus doses prophylactiques.
Récemment, une étude européenne incluant un grand nombre de patients (3002 patients randomisés) et publiée dans une revue médicale de grande qualité, a pour la première fois montré le bénéfice d’un protocole d’anticoagulant dans le traitement des TVS en comparant le fondaparinux à doses prophylactiques 2,5 mg 1 injection/jour pendant 45 jours versus un placebo [4]. La différence de survenue d’évènements TEV était statistiquement très significative (0,9% vs 5,9 % ; p < 0,001), sans augmentation du risque hémorragique ou autres complications. Il est cependant intéressant de noter que les complications TEV étaient relativement peu fréquentes dans le groupe placébo.
Cette étude nommée « Calisto » a conduit à établir de nouvelles recommandations internationales [5,6] dans le traitement des TVS symptomatiques isolées (sans TVP ni EP) des membres inférieurs, faisant plus de 5 cm de longueur et n’atteignant pas la jonction saphéno-fémorale, en préconisant l’usage d’un traitement anticoagulant à doses prophylactiques pendant 45 jours (grade 2 B) et de préférence le fondaparinux 2,5 mg par jour (grade 2C).
Ces recommandations sont d’un faible grade (2B et 2C), car elles sont basées sur une seule étude et, car elles prennent en compte un taux relativement faible d’évènements TEV dans le groupe placebo.
En parallèle, une compression élastique doit être appliquée et la marche est recommandée.
Dans le cas particulier des TVS étendues à la jonction saphéno-fémorale ou saphéno-poplitée, un traitement anticoagulant à doses curatives pendant 3 mois est recommandé (avis d’experts).
EN CONCLUSION
La prise en charge actuelle des TVS des membres inférieurs peut se résumer en 2 messages principaux:
- nécessité d’un examen écho-doppler en urgence (pour affirmer le diagnostic, préciser l’extension de la TVS notamment à la jonction saphéno-fémorale ou saphéno-poplitée et rechercher une éventuelle TVP associée) ;recherche d’un embolie pulmonaire si extention du thrombus
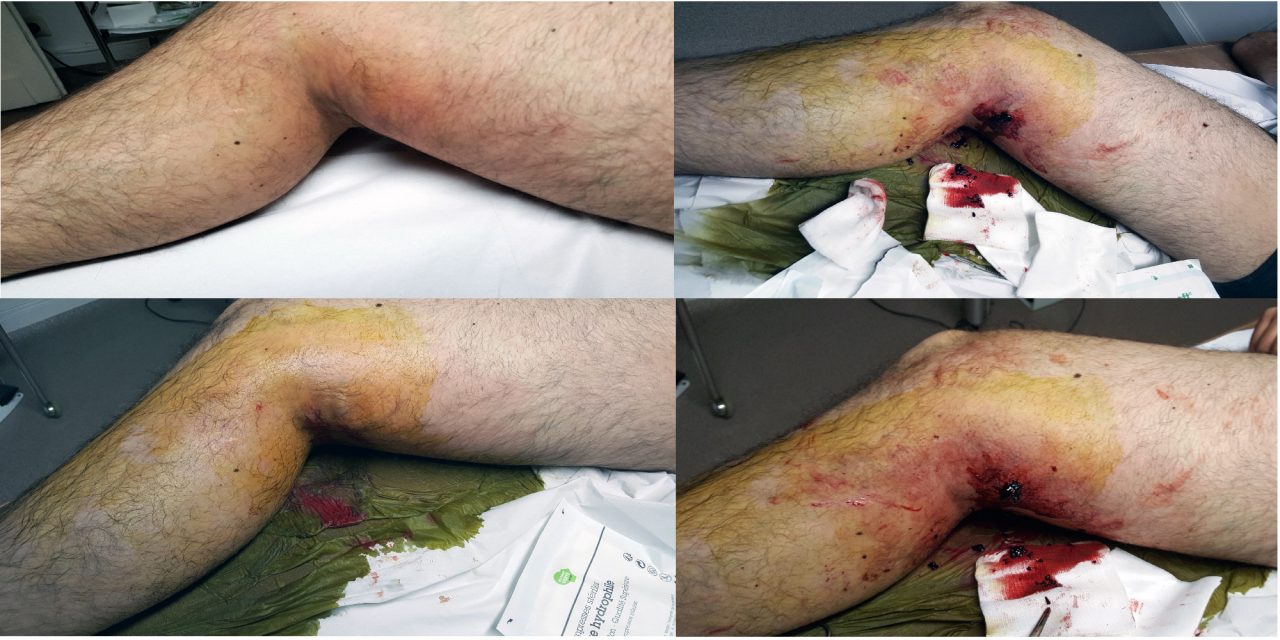
- si trop douloureux, on peut faire une évacuation du thrombus pour diminuer la compression ,sous anesthésie locale
- [easingslider id= »1297″]
- dans le cas d’une TVS faisant au moins 5 cm de long : traitement anticoagulant à doses prophylactiques, de préférence fondaparinux 2,5 mg/jour, pendant 45 jours.
Cliquer ici pour ajouter votre propre texte